
Guía Clínica por Madrid Urología
Introducción y Magnitud del Problema
El síndrome doloroso pélvico crónico (SDPC), también conocido como prostatitis crónica categoría III según la clasificación del NIH, es una de las patologías urológicas más frecuentes en varones jóvenes, representando aproximadamente el 90-95% de todos los casos de prostatitis.[1] Esta condición se caracteriza por dolor pélvico persistente durante al menos 3 meses, localizado en periné, región suprapúbica, testículos, pene o asociado a la micción y eyaculación, en ausencia de infección bacteriana demostrable.[2][3]

La disfunción sexual es una comorbilidad extremadamente prevalente en estos pacientes, afectando significativamente su calidad de vida y relaciones interpersonales. Los estudios demuestran que hasta el 62% de los varones con SDPC presentan algún tipo de disfunción sexual, siendo las más frecuentes la disfunción eréctil (DE) y la eyaculación precoz (EP).[4]
Prevalencia de Disfunciones Sexuales en SDPC
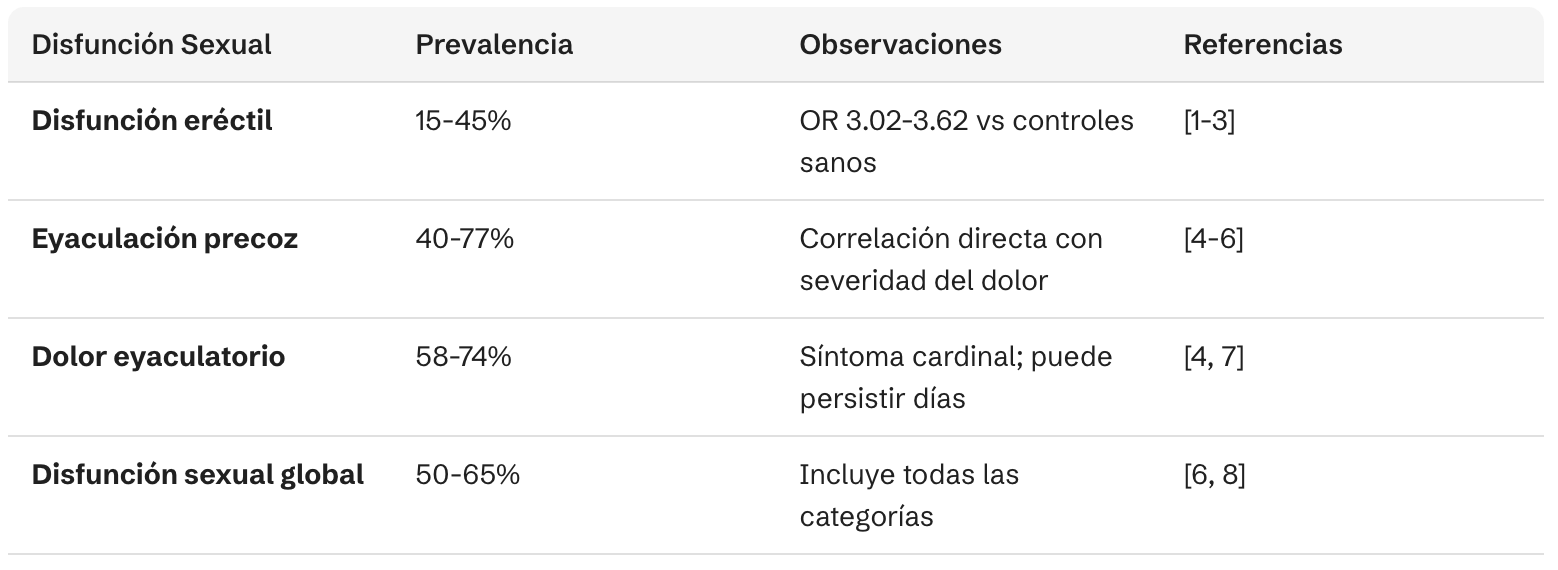
Disfunción Eréctil y SDPC
La asociación entre SDPC y disfunción eréctil está firmemente establecida. Un metaanálisis de 9 estudios con 31,956 participantes demostró que los pacientes con SDPC tienen un riesgo 3 veces mayor de desarrollar DE (OR: 3.02; IC 95%: 2.18-4.17) comparado con controles sanos.[5] Estudios poblacionales confirman esta asociación, con un OR de 3.62 (IC 95%: 3.07-4.26) tras ajustar por factores de confusión como hipertensión, diabetes y enfermedad coronaria.[7]
La prevalencia de DE en pacientes con SDPC oscila entre el 15% y el 45%, dependiendo de la población estudiada y los criterios diagnósticos utilizados.[6][2] Un estudio multicéntrico con 1,406 pacientes encontró DE en el 45.4% de los casos, clasificada como leve (45.6%), moderada (46.6%) y severa (7.7%).[6]
Los factores de riesgo independientes para DE en pacientes con SDPC incluyen:
- Dominio psicológico del sistema UPOINT
- Severidad de los síntomas según NIH-CPSI
- Depresión y estrés
Eyaculación Precoz y SDPC
La eyaculación precoz es particularmente prevalente en varones con SDPC, con tasas que oscilan entre el 40% y el 77% según diferentes estudios.[2][8][4] Un estudio poblacional con 8,261 hombres demostró una correlación significativa entre la puntuación del PEDT (Premature Ejaculation Diagnostic Tool) y el dominio de dolor del NIH-CPSI (coeficiente de correlación = 0.206; p < 0.001).[8]
La relación es dosis-dependiente: a mayor severidad del dolor pélvico, mayor riesgo de EP:
- Síntomas leves de prostatitis: OR 1.27 (IC 95%: 1.11-1.45)
- Síntomas moderados-severos: OR 2.13 (IC 95%: 1.78-2.56)[8]
Esta asociación se mantiene incluso después de ajustar por edad, síndrome metabólico, niveles de testosterona y función eréctil, lo que sugiere una relación fisiopatológica directa entre la inflamación prostática crónica y la disfunción eyaculatoria.[8]
Dolor Eyaculatorio: Un Síntoma Cardinal
El dolor con la eyaculación es uno de los síntomas más característicos y debilitantes del SDPC, presente en el 58-74% de los pacientes.[2][9] Este síntoma tiene implicaciones pronósticas importantes:
Los pacientes con dolor eyaculatorio persistente presentan:
- Puntuaciones NIH-CPSI significativamente más altas (25.5 vs 18.5 en pacientes sin dolor eyaculatorio)
- Peor calidad de vida física y mental
- Menor probabilidad de mejoría espontánea con el tiempo
- Mayor variedad de prácticas sexuales como intento de evitar el dolor[9]
El dolor puede ser tan intenso que las molestias persisten durante horas o incluso días después de la eyaculación, lo que lleva a muchos pacientes a evitar completamente la actividad sexual.[9][11]
Impacto en la Fertilidad
El SDPC tiene un efecto deletéreo significativo sobre los parámetros seminales y la fertilidad masculina. Un metaanálisis reciente demostró las siguientes alteraciones:[12][13] SMD: Diferencia de Medida Estandarizada.
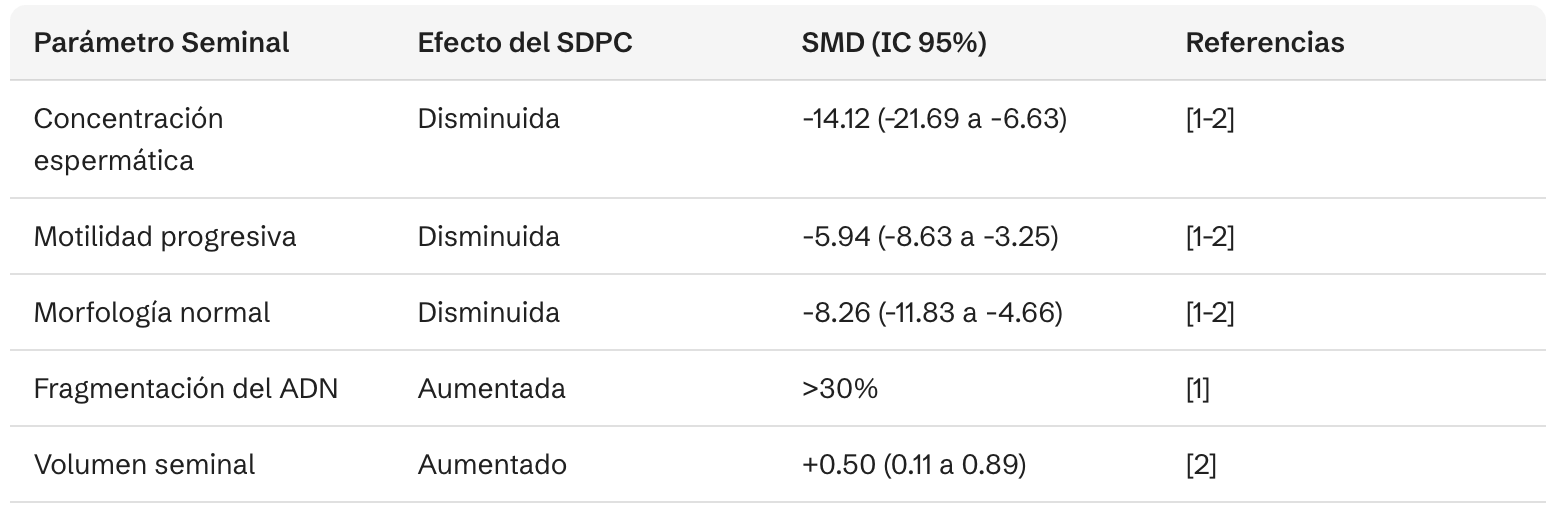
Los mecanismos propuestos incluyen:[12][14][15]
1. Citoquinas proinflamatorias (IL-6, TNF-?) que dańan la función mitocondrial y la integridad del ADN espermático
2. Disfunción neuroendocrina que inhibe el eje hipotálamo-hipófisis-testicular
3. Disminución de zinc en plasma seminal (SMD: -20.73; p = 0.005)
4. Producción de anticuerpos anti-espermatozoides (OR: 3.26; p < 0.01)
5. Respuestas autoinmunes Th1 y Th17 específicas contra antígenos prostáticos y seminales[15]
Impacto Psicológico y en las Relaciones de Pareja
El SDPC, al ser una enfermedad que afecta predominantemente a varones jóvenes (edad media 32 ańos), tiene consecuencias devastadoras en las relaciones interpersonales y la calidad de vida.[6][10]
Los pacientes con SDPC presentan:
- Mayor prevalencia de depresión (12-33% cumplen criterios de depresión mayor)[16]
- Ansiedad y aislamiento social como consecuencia del dolor crónico[16]
- Deterioro de la calidad de las relaciones sexuales comparado con controles sanos y pacientes con otros síndromes de dolor crónico[10]
- Evitación de relaciones sexuales por miedo al dolor o a la disfunción[9]
La depresión, el estrés y el dolor genital son predictores independientes tanto de DE como de disfunción eyaculatoria en análisis multivariados.[10] Además, existe una relación bidireccional: la disfunción sexual empeora la depresión, y la depresión amplifica la percepción del dolor y la disfunción sexual, creando un círculo vicioso difícil de romper.[16][17]
Mecanismos Fisiopatológicos de la Disfunción Sexual en SDPC
La disfunción sexual en el SDPC es multifactorial:[18][12]
1. Inflamación crónica prostática: Las citoquinas proinflamatorias (IFN?, IL-17, IL-1?, IL-8) y la infiltración leucocitaria (linfocitos T CD4, macrófagos) generan un ambiente inflamatorio local que afecta la función sexual.[18][15]
2. Sensibilización neural: La inflamación crónica induce sensibilización de las vías nerviosas pélvicas, amplificando la percepción del dolor y alterando los reflejos eyaculatorios.[18]
3. Disfunción del suelo pélvico: La hipertonía muscular pélvica asociada al SDPC contribuye tanto al dolor como a la disfunción eréctil y eyaculatoria.[19]
4. Factores psicológicos: La ansiedad anticipatoria, la catastrofización del dolor y la depresión modulan negativamente la respuesta sexual.[6][10]
5. Alteraciones hormonales: Aunque menos estudiadas, pueden existir alteraciones en el eje neuroendocrino que afecten la función sexual.[12]
Recomendaciones Clínicas
Dado el alto impacto de la disfunción sexual en pacientes con SDPC, se recomienda:[8][19][17]
1. Evaluación sistemática de la función sexual en todo paciente con diagnóstico de SDPC, utilizando cuestionarios validados (IIEF-5, PEDT)
2. Cribado de SDPC en pacientes con eyaculación precoz, especialmente si es adquirida, dado que el OR para EP aumenta significativamente con la severidad del dolor pélvico[8]
3. Abordaje multidisciplinario que incluya:
- Tratamiento del dolor pélvico
- Manejo de la disfunción sexual específica
- Apoyo psicológico/terapia cognitivo-conductual
- Rehabilitación del suelo pélvico[17][20]
4. Evaluación de la fertilidad en pacientes con deseo genésico, dado el impacto negativo sobre los parámetros seminales[12][14]
5. Comunicación abierta con la pareja y consideración de terapia de pareja cuando sea apropiado[20]
Conclusión
El síndrome doloroso pélvico crónico es mucho más que dolor pélvico: es una condición que afecta profundamente la sexualidad, la fertilidad y la calidad de vida de los varones jóvenes. La disfunción eréctil, la eyaculación precoz y el dolor eyaculatorio son comorbilidades frecuentes que deben ser activamente buscadas y tratadas. El reconocimiento de esta asociación y su abordaje integral son fundamentales para mejorar los resultados clínicos y la satisfacción del paciente.
References
- Chronic Prostatitis and the Chronic Pelvic Pain Syndrome. Schaeffer AJ. The New England Journal of Medicine. 2006;355(16):1690-8. doi:10.1056/NEJMcp060423.
- Prostatitis. Borgert BJ, Wallen EM, Pham MN. JAMA. 2025;334(11):1003-1013. doi:10.1001/jama.2025.11499.
- What Is Prostatitis?. Voelker R. JAMA. 2026;:2843664. doi:10.1001/jama.2025.20559.
- Prevalence of Sexual Dysfunction in Men With Chronic Prostatitis/Chronic Pelvic Pain Syndrome: A Meta-Analysis. Li HJ, Kang DY. World Journal of Urology. 2016;34(7):1009-17. doi:10.1007/s00345-015-1720-3.
- The Effect of Chronic Prostatitis/Chronic Pelvic Pain Syndrome (CP/CPPS) on Erectile Function: A Systematic Review and Meta-Analysis. Chen X, Zhou Z, Qiu X, Wang B, Dai J. PloS One. 2015;10(10):e0141447. doi:10.1371/journal.pone.0141447.
- Erectile Dysfunction in Chronic Prostatitis/Chronic Pelvic Pain Syndrome: Outcomes From a Multi-Center Study and Risk Factor Analysis in a Single Center. Zhang Y, Zheng T, Tu X, et al. PloS One. 2016;11(4):e0153054. doi:10.1371/journal.pone.0153054.
- A Case-Control Study on the Association Between Chronic Prostatitis/Chronic Pelvic Pain Syndrome and Erectile Dysfunction. Chung SD, Keller JJ, Lin HC. BJU International. 2012;110(5):726-30. doi:10.1111/j.1464-410X.2011.10807.x.
- Relationship Between Premature Ejaculation and Chronic Prostatitis/Chronic Pelvic Pain Syndrome. Lee JH, Lee SW. The Journal of Sexual Medicine. 2015;12(3):697-704. doi:10.1111/jsm.12796.
- Impact of Post-Ejaculatory Pain in Men With Category III Chronic Prostatitis/Chronic Pelvic Pain Syndrome. Shoskes DA, Landis JR, Wang Y, et al. The Journal of Urology. 2004;172(2):542-7. doi:10.1097/01.ju.0000132798.48067.23.
- Predictors of Male Sexual Dysfunction in Urologic Chronic Pelvic Pain Syndrome (UCPPS), Other Chronic Pain Syndromes, and Healthy Controls in the Multidisciplinary Approach to the Study of Chronic Pelvic Pain (MAPP) Research Network. Loh-Doyle JC, Stephens-Shields AJ, Rolston R, et al. The Journal of Sexual Medicine. 2022;19(12):1804-1812. doi:10.1016/j.jsxm.2022.08.196.
- Painful Ejaculation. Ilie CP, Mischianu DL, Pemberton RJ. BJU International. 2007;99(6):1335-9. doi:10.1111/j.1464-410X.2007.06664.x.
- Chronic Prostatitis and Male Infertility: Association Mechanism and Research Progress. Qinyu Z, Jitao S, Yang X, Yue D, Hao Z. World Journal of Urology. 2025;43(1):599. doi:10.1007/s00345-025-05964-z.
- The Effect of Chronic Prostatitis/Chronic Pelvic Pain Syndrome (CP/CPPS) on Semen Parameters in Human Males: A Systematic Review and Meta-Analysis. Fu W, Zhou Z, Liu S, et al. PloS One. 2014;9(4):e94991. doi:10.1371/journal.pone.0094991.
- Chronic Prostatitis and Its Detrimental Impact on Sperm Parameters: A Systematic Review and Meta-Analysis. Condorelli RA, Russo GI, Calogero AE, Morgia G, La Vignera S. Journal of Endocrinological Investigation. 2017;40(11):1209-1218. doi:10.1007/s40618-017-0684-0.
- Patients With Chronic Prostatitis/Chronic Pelvic Pain Syndrome Show T Helper Type 1 (Th1) and Th17 Self-Reactive Immune Responses Specific to Prostate and Seminal Antigens and Diminished Semen Quality. Motrich RD, Breser ML, Molina RI, et al. BJU International. 2020;126(3):379-387. doi:10.1111/bju.15117.
- Chronic Pelvic Pain: ACOG Practice Bulletin, Number 218. Obstetrics and Gynecology. 2020;135(3):e98-e109. doi:10.1097/AOG.0000000000003716.
- Chronic Pelvic Pain in Women: A Review. Lamvu G, Carrillo J, Ouyang C, Rapkin A. JAMA. 2021;325(23):2381-2391. doi:10.1001/jama.2021.2631.
- Immunological Mechanisms Underlying Chronic Pelvic Pain and Prostate Inflammation in Chronic Pelvic Pain Syndrome. Breser ML, Salazar FC, Rivero VE, Motrich RD. Frontiers in Immunology. 2017;8:898. doi:10.3389/fimmu.2017.00898.
- Acute and Chronic Prostatitis. Lam JC, Stokes W. American Family Physician. 2024;110(1):45-51.
- Chronic Pelvic Pain in Women: Evaluation and Treatment. Meisenheimer ES, Carnevale AM. American Family Physician. 2025;111(3):218-229.
???Consultas Urológicas Madrid Urología
??Madrid Urología ??
?Aquí es Donde la Solución Empieza?
? Consultas 100 % privadas. La mejor atención garantizada.
? Consultas de 1 hora.
? Cirugía en 3 días
? Calle Corazón de María 23. Primero B. Chamartín. Madrid. Espańa